Коррозией металлов называется самопроизвольное их разрушение вследствие химического или электрохимического взаимодействия с окружающей средой.
Химическая коррозия – это процесс, при котором окисление металла и восстановление окислительного компонента среды протекают в одном акте. Типичный пример: окисление железа кислородом воздуха:
2 Fе + O2 2 FeO
Наиболее распространенным и практически важным видом химической коррозии является газовая коррозия – коррозия металлов в газах при высоких температурах.
Электрохимическая коррозия – это разрушение металлов вследствие их электрохимического взаимодействия с электролитически проводящей средой, при котором ионизация атомов металла и восстановление окислительного компонента среды протекает не в одном акте и их скорости зависят от величины электродного потенциала металла. Этот вид коррозии наиболее распространен и является превалирующим для интересующих нас условий эксплуатации металлоконструкций. Первопричиной коррозии металлов является их термодинамическая неустойчивость в различных средах при данных внешних условиях. Термодинамика определяет возможность или невозможность самопроизвольного протекания коррозионного процесса при определенных условиях.
Скорость коррозионного процесса может быть представлена в общем виде с помощью уравнения:
Скорость коррозии (СК) = Движущая сила процесса (ДСП)/Торможение процесса (ТП)
ДСП может быть определена с помощью термодинамики. ТП не может быть определено термодинамически, однако с помощью термодинамики можно оценить условия, уменьшающие или исключающие протекание процесса (применение защитных сред, катодная защита, обескислороживание и др.).
Независимо от механизма коррозии возможность ее протекания определяется знаком изменения термодинамического потенциала. Процессы коррозии наиболее часто описывают изменением изобарно-изотермического потенциала – энергии Гиббса.
Любое изменение энергии системы характеризует переход ее в новое состояние и является мерой стабильности системы:
ΔG = GII – GI,
где ΔG – энергия, израсходованная на изменение состояния системы, например, на процесс коррозии; GI – энергия системы в исходном состоянии, например, металла в конкретных условиях; GII – энергия системы в новом состоянии, например, прокорродировавшего металла.
Очевидно, что при ΔG = 0 система находится в равновесии; при ΔG < 0 процесс коррозии возможен при ΔG > 0 процесс коррозии невозможен.
Процесс электрохимической коррозии включает в себя пять основных этапов. Например, для случая коррозии углеродистой стали в воде или влажном воздухе процесс протекает следующим образом:
- ионизация атомов железа с образованием гидратированных ионов в воде и некомпенсированных электронов на анодных участках металла Fe + mH2O Fe+2mH2O + 2е–;
- переход электронов на катодные участки и их ассимиляция деполяризаторами (в нейтральных растворах кислородом) с образованием ионов гидроксила O2+2Н2O + 4е– 4 ОН–;
- образование в растворе гидрата закиси железа Fe2+ + 2 ОН– Fe(OH)2;
- доокисление до гидрата окиси железа Fe (ОH)3 и преобразование его в окончательный продукт коррозии Fe2О3 mH2O.
Суммарная реакция коррозии стали будет иметь вид:
4 Fe+ mH2O + 3O2 2 Fe2O3 * mH2O,
Коррозия металла представляется как результат работы большого числа коррозионных гальванических элементов, возникающих на отдельных участках поверхности вследствие ее гетерогенности. Электрохимическая гетерогенность поверхности металла, обусловливающая ее дифференциацию на анодные и катодные участки, может быть вызвана различными причинами; макро- и микровключениями примесей, анизотропностью кристаллической решетки, наличием оксидных пленок и других загрязнений, неравномерностью приложения механических нагрузок, наличием пар дифференциальной аэрации и др.
Скорость и характер коррозионного процесса определяется в конечном итоге величиной стационарного потенциала металла φ, отвечающей установившейся скорости ионизации металла.
Усредненные значения стационарных потенциалов металлов в морской воде (по водородному электроду, В*) можно расположить в ряд:
| Магний | -1,45 | Олово | -0,20 |
| Марганец | -0,96 | Медь | -0,10 |
| Цинк | -0,80 | Титан | 0 |
| Алюминий | -0,54 | Ниобий | +0,10 |
| Железо | -0,40 | Никель | +0,10 |
| Кадмий | -0,40 | Серебро | +0,15 |
| Свинец | -0,30 | Платина | +0,80 |
Исходя из теории локальных элементов ток коррозии в общем виде может определяться по закону Ома:
Ik = (фk - фa)/(Rnk+Rna+Rom)
где (φk., φа – потенциалы катодных и анодных участков): RnK, Rna – соответственно поляризационное сопротивление на катоде и аноде; Roм – сопротивление электролита.
Определяющие скорость коррозии соотношения обычно наглядно представляются в виде коррозионных диаграмм (рис.), где потенциалы анода и катода представляются в функции силы тока.
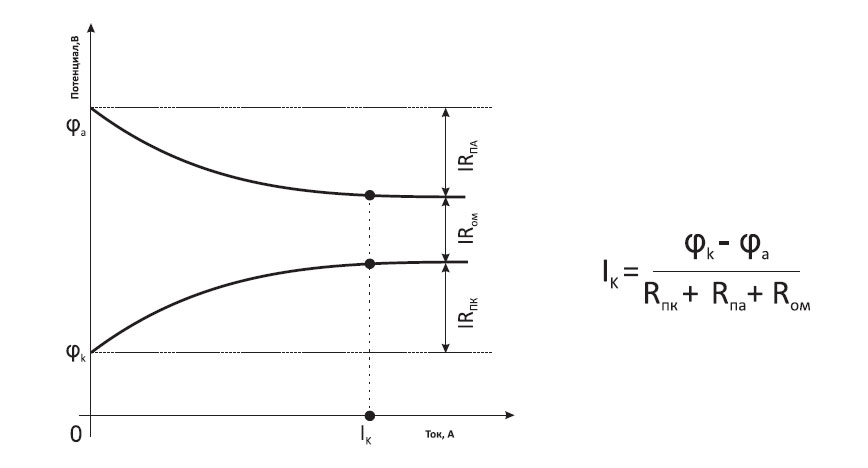
Рис. Диаграмма для расчета тока коррозии.
Чаще всего скорость коррозионного процесса определяется следующими факторами:
- медленностью диффузии реагентов к поверхности металла или продуктов реакции в обратном направлении (диффузионный контроль процесса);
- медленностью реакции взаимодействия металла с коррозионной средой или ее компонентами, обусловленной энергией активации реакции (кинетический контроль);
- медленностью обеих стадий при соизмерении их торможений (диффузионно-кинетический контроль).
* Здесь и далее величины потенциалов даны по водородному электроду. На практике обычно применяются хлорсеребряные электроды сравнения, имеющие собственный потенциал +240 мВ по отношению к нормальному водородному электроду, реже медносульфатные +310 мВ и цинковые – 800 мВ.
Надежную защиту коррозии металла обеспечит холодное цинкование.

